衡水金卷先享题摸底卷2023-2024学年度高三一轮复习摸底测试卷(三)历史考试试卷
衡水金卷先享题摸底卷2023-2024学年度高三一轮复习摸底测试卷(三)历史试卷答案,我们目前收集并整理关于衡水金卷先享题摸底卷2023-2024学年度高三一轮复习摸底测试卷(三)历史得系列试题及其答案,更多试题答案请关注本网站

衡水金卷先享题摸底卷2023-2024学年度高三一轮复习摸底测试卷(三)历史试卷答案
以下是该试卷的部分内容或者是答案亦或者啥也没有,更多试题答案请关注本网站
C.HC1O3的酸性比H2SO3的强BD.向H2S水溶液中通入Cl2有淡黄色沉淀生成*E.硫化氢在300℃时开始分解,HCI在1500℃时开始缓慢分解【答案】(1)第三周期IA族(2分)8Si(1分分个(2)Na[:O:O:]2-Na+(2分):Cl:O:C:(2分)(3)Be+2NaOH-Na2BeO2+H2↑(2分)(4)BDE(2分)【解析】(1)已知Na为11号元素,电子排布式为1s22s22p3s2,故在周期表中的位置是第三周期IA族,硅为14号元素,质子数为14,根据质量数=质子数十中子数,故质子数与中子数相等的硅原子符号为8Si,钙是20号元0【装督】素,故钙离子的结构示意图餐体转(2)根据电子式的书写原则可知,Na2O2是离子化合物,故Na2O2的电子式为Na+[:O:0:]?-Na+,Cl20是共价化合物,故C2O的电子式为:C1:O:C:
(3)Be与Al的化学性质相似,根据Al与NaOH溶液反应生成NaA1O2和H2可知,由于Be的最外层上只有2个电子,故显+2价,则Be与NaOH溶液反应的化学方程式是Be十2NaOH—Na2BeO2十H2↑
(4)氯、硫的最低负化合价分别为一1、一2,只能说明C1元素能够得到1个电子,而S元素能得到2个电子,非金属性与得电子的难易程度有关,与得电子的多少无关,A不符合题意;S2CL2中氯显一1价,硫显十1价,说明S的电负性比C1的弱,电负性越大,非金属性越强,B符合题意;非金属元素的最高价氧化物对应水化物的酸性与非金属性一致,HCIO3和H2SO3均不是Cl和S的最高价氧化物对应的水化物,故HCIO3的酸性比H2SO3的强不能说明Cl的非金属性比S强,C不符合题意;向H2S水溶液中通入Cl2有淡黄色沉淀生成,反应为H2S十Cl2一2HCl十S↓,说明C2的氧化性比S的强,故说明CI的非金属性比S的强,D符合题意;非金属元素的简单氢化物的热稳定性与非金属性一致,故硫化氢在300℃时开始分解,HC1在1500℃时开始缓慢分解,说明HCl比H2S稳定,即CI的非金属性强于S,E符合题意
18.(13分)为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”
回答下列问题:(1)据汞的原子结构示意图81832182,汞在第4周期
(2)NH、H2O、H2S分别为氮、氧、硫3种元素对应的简单氢化物,简单氢化物的稳定性顺序为>地的行金诗(3)下列有关性质的比较能用元素周期律解释的是(填字母,下同)
a.酸性:HCI>H2S0g中b.非金属性:O>Sc.碱性:NaOH>Mg(OH)d.热稳定性:Na2CO3>NaHCO3量(4)硒(S)与硫位于同一主族,均是生命必需元素
下列推断正确的是a.硒元素的最低负化合价为一2b.二氧化硒(SeO2)具有还原性c.硒的氧化物对应的水化物属于强酸·82·

2.司马迁的《史记》和班固的《汉书》都有关于民族史的撰述,《史记》不斤斤于夷夏之别,肯定华夷各族同源共祖的思想尤为进步,而《汉书》的“异内外”和“德化四夷”的“别夷夏”色彩较为浓厚,以羁縻的办法对待夷狄也显得无为消极。对二者民族史撰述思想的差异说法最准确的是(A.侧面反映了汉代政治局势变化B.治史修养的不同是主要原因C.说明司马迁史学研究成就更太D.体现了东汉不注重民族治理
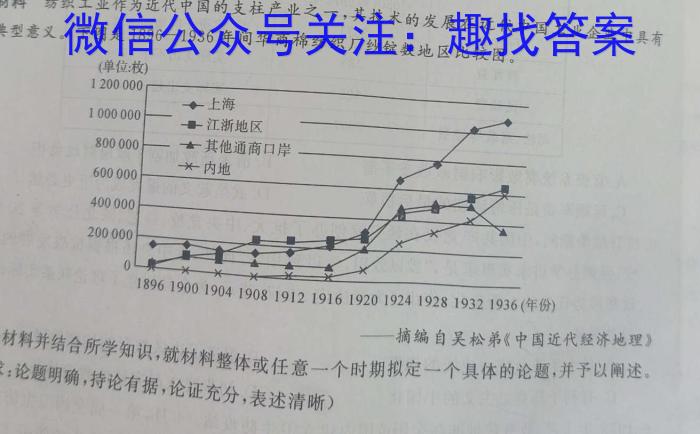
19.阅读材料,完成下列要求。(12分)材料纺织工业作为近代中国的支柱产业之一,其技术的发展在近代中国工业企业中具有典型意义。下图是1896一1936年间华商棉纺织厂纱锭数地区比较图。18961901904190819121916192201924192819321936(年份)——摘编自吴松弟《中国近代经济地理》根据材料并结合所学知识,就材料整体或任意一个时期拟定一个具体的论题,并予以阐述。(要求:论题明确,持论有据,论证充分,表述清晰)

相关文章
- 陕西省咸阳市永寿县中学2024年高三质量检测卷(24474C)物理考试试卷
- 2024届阳光启学全国统一考试标准模拟信息(七)物理考试试卷
- 安徽省宿州市萧县2023-2024学年度九年级第一次模考物理考试试卷
- “皖韵风华·智慧挑战”九年级安徽省联盟考试物理考试试卷
- 2024年陕西省初中学业水平考试·全真模拟卷(二)物理考试试卷
- 江西省2023-2024学年度八年级下学期第一阶段练习物理考试试卷
- 湖北省2024届高中毕业生四月模拟考试物理考试试卷
- 顶尖联盟2024届高中毕业班第三次考试(老教材版)物理考试试卷
- 2024年河南省普通高中招生考试模拟卷(一)物理考试试卷
- 山西省2023-2024学年七年级3月份单元诊断物理考试试卷

